Как было сказано в главе про строение атома, в них есть энергетические уровни. Эту тему необходимо разбирать отдельно, так как она довольно емкая.
Энергетические уровни - уровни, на которых располагаются электроны. Уровни делятся на подуровни.
Энергетические подуровни - части энергетического уровня, на которых располагаются различные атомные орбитали.
Далее приведу шкалу энергетических уровней и подуровней:
1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p и т.д.
Атомные орбитали - пространство, в котором будет находиться данный электрон с наибольшей долью вероятности. Различают s-, p-, d- и f-орбитали.

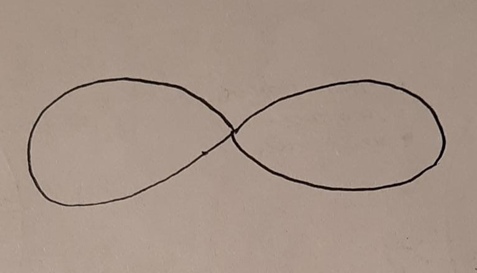
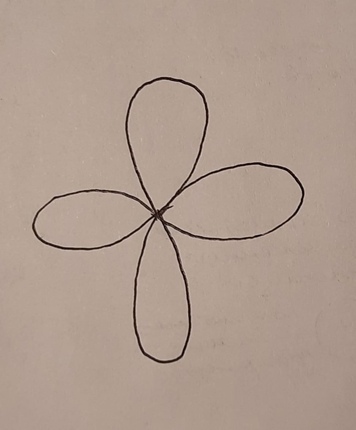

p-, d- и f-орбитали также могут быть наклонены различным образом по осям x, y и z.
Химики договорились, что характеристика атомов элементов будет приводиться с помощью квантовых чисел.
Различают 4 вида квантовых чисел: главное, побочное, магнитное и спиновое.
Главное квантовое число (n) - число, которое показывает количество энергетических уровней в атоме данного элемента. Оно может принимать значения
от 1 до n (числа принадлежат множеству Z) и равно номеру периода, в котором находится данный элемент.
Побочное квантовое число (l) - число, которое показывает тип атомной орбитали. Его значение может принимать значения от 0 до (n-1).
Как понять тип атомной орбитали по побочному квантовому числу?
если l = 0, то это s-орбиталь
если l = 1, то это p-орбиталь
если l = 2, то это d-орбиталь
если l = 3, то это f-орбиталь
Магнитное квантовое число (m) - число, которое показывает, как наклонена атомная орбиталь относительно координатной плоскости. Число принимает
значения от -l, ..., 0; ..., l; все числа принадлежат множеству Z.
Спиновое квантовое число (ms(s - индекс)) - число, которое показывает, в какую сторону вращается электрон в данном атоме. Принимает только значения
-1/2 и +1/2. Если ms = -1/2, то электрон вращается в левую сторону, а если ms = +1/2, то в правую.
По правилу Хунда в атоме сумма спинов электронов должна быть максимальной, поэтому в атоме электронов со спином, равным +1/2 больше или равно
количеству электронов со спином, равным -1/2.
В атоме зачастую есть электроны с антипараллельными спинами (+1/2 и -1/2). Такие электроны называются спаренными.